近日,上海交通大学医学院附属同仁医院乳腺外科周竹超、汪洁团队联合苏州大学在高水平学术期刊 《Advanced Materials》(影响因子26.8)发表题为 “Potentiating Antibody-Dependent Cell-Mediated Cytotoxicity via Tumor-Specific Anchoring and Activation of Nano-Haptens”的研究论文。该研究聚焦实体瘤免疫治疗中的一个关键难题:虽然人体内的自然杀伤细胞(NK细胞)具有识别并清除肿瘤细胞的能力,但在实体瘤中(比如三阴性乳腺癌)这种杀伤作用常常因为肿瘤表面标志物不足、肿瘤微环境免疫抑制强等原因而受到限制。针对这一问题,研究团队设计了一种能够在肿瘤局部被“精准激活”的纳米系统,使其先在肿瘤细胞表面稳定“锚定”,再进一步招募并增强NK细胞的杀伤功能,从而更有效地放大机体自身的抗肿瘤免疫反应。研究结果表明,这一策略不仅能够显著提升对肿瘤的清除效果,还有望为实体瘤免疫治疗提供新的思路和潜在方案。

抗体依赖的细胞介导细胞毒作用(ADCC)是肿瘤免疫治疗的重要机制之一,其本质是借助抗体将肿瘤细胞与自然杀伤细胞(NK细胞)连接起来,进而激活NK细胞对肿瘤细胞的杀伤作用。然而在实体瘤中,受肿瘤表面抗原异质性较高、肿瘤微环境免疫抑制明显等因素影响,ADCC效应往往难以充分发挥。如何更有效地激活NK细胞、提升其对实体瘤的清除能力,已成为肿瘤免疫治疗领域关注的重要问题。
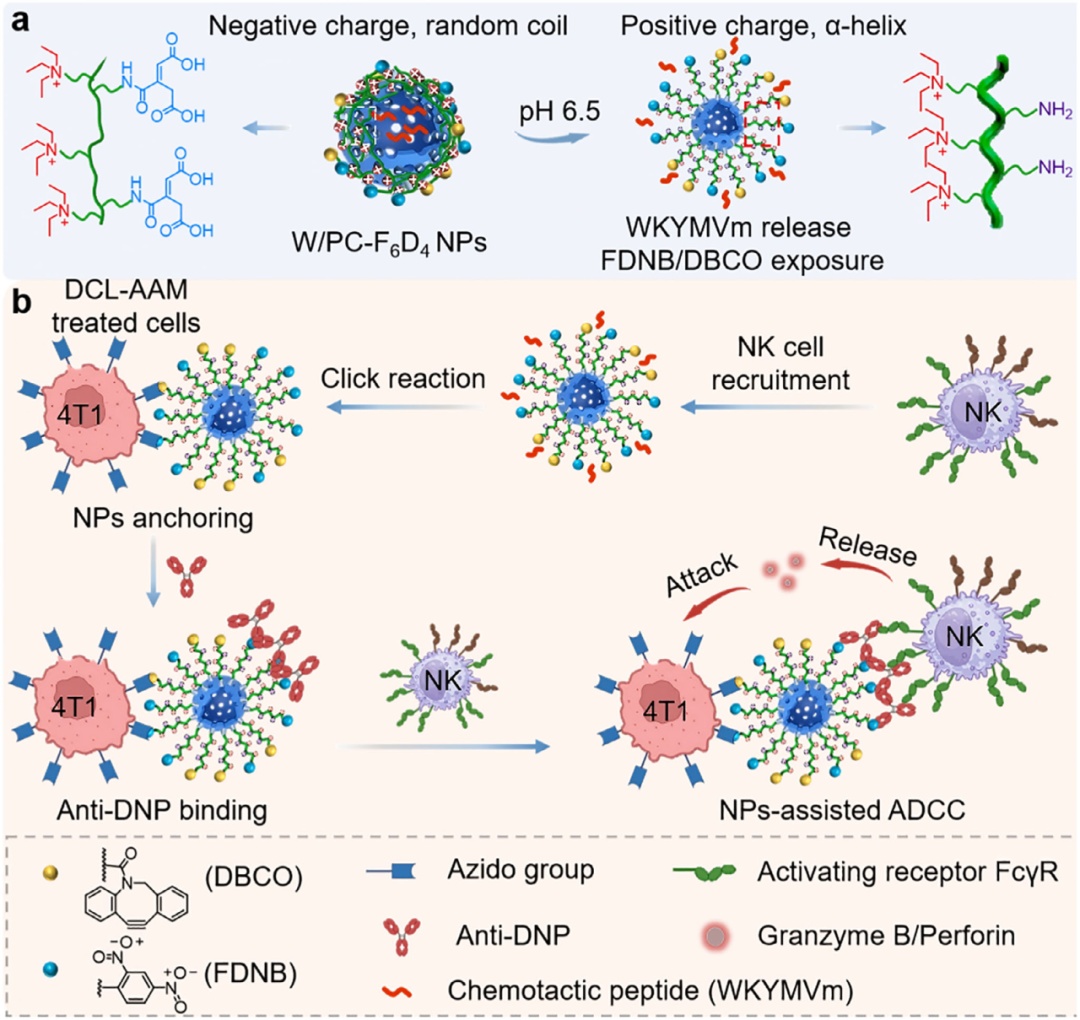
针对上述难题,研究团队构建了一种可在肿瘤局部精准激活的酸响应纳米半抗原系统。该系统通过代谢糖工程在肿瘤细胞表面引入可识别位点,再借助肿瘤微环境特征实现纳米系统的选择性激活和稳定锚定,同时增强内源性抗体募集及NK细胞浸润,进而放大ADCC抗肿瘤效应。该策略将“肿瘤识别、局部激活、免疫桥接”有机整合,强化自身免疫实现抗肿瘤,而避免了化疗等细胞毒性药物治疗带来的副作用,为实体瘤免疫治疗提供了新的技术路径。
该研究的一大亮点在于实现了纳米系统在体内的“按需激活”。在血液循环过程中,纳米系统保持相对稳定和隐蔽状态,避免关键功能基团过早暴露;进入偏酸性的肿瘤微环境后,材料结构发生响应性转变,逐步暴露功能位点。一方面,系统可释放相关分子,促进NK细胞向肿瘤部位聚集;另一方面,可精准锚定于肿瘤细胞表面,并结合内源性抗体,在肿瘤细胞与NK细胞之间建立更高效的免疫连接,从而增强NK细胞介导的杀伤效应。该研究不仅通过纳米半抗原实现肿瘤细胞与NK细胞之间的高效桥接,增强ADCC效应,还进一步阻断NK细胞表面的Ly49C受体,阻止肿瘤细胞利用MHC-I分子向NK细胞传递“别杀我”的抑制信号,从而恢复并增强NK细胞对肿瘤的杀伤能力。
研究结果表明,该策略在体外和体内均展现出良好的抗肿瘤效果。实验发现,该纳米系统能够显著提升三阴性乳腺癌细胞表面的锚定效率,增强抗体结合能力,并促进NK细胞与肿瘤细胞之间的有效接触,从而提高ADCC水平。在动物模型中,该策略进一步表现出更好的肿瘤部位富集能力和免疫激活效果,可显著抑制肿瘤生长并延长生存时间。联合相关免疫调控策略后,其抗肿瘤作用还可进一步增强。
该研究为实体瘤免疫治疗提供了新的思路,即通过人工构建可识别、可激活、可桥接的肿瘤表面免疫界面,突破传统ADCC在实体瘤中效应受限的瓶颈。该工作有机融合了材料设计、生物正交化学、代谢糖工程与肿瘤免疫调控,不仅体现出较强的创新性,也展现出良好的应用潜力,为未来开发更精准、高效的实体瘤免疫治疗策略提供了有价值的参考。
我院乳腺外科周竹超教授、苏州大学功能纳米与软物质研究院殷黎晨副院长为该论文通讯作者。周竹超教授近年在利用纳米技术攻克三阴性乳腺癌靶向和免疫治疗领域已发表多篇顶刊(Advanced Healthcare Materials 2024,Chemical Engineering Journal 2024,Nano Today 2025等)。该研究受到多项国家自然科学基金的资助。
供稿:周竹超
审核:汪 洁、岳静雯
校审:张韵明
预约就诊请关注公众号:
(部分图片源自网络,如有侵权请通知删除)
TONGREN HOSPITAL
欢迎关注同仁医院官方微信服务号