
近期,浦东创新药企的医疗器械成果持续涌现:跨国药企葛兰素史克的创新疗法在华获批、复宏汉霖公布7项创新成果、上海微创医疗器械(集团)有限公司自主研发的新一代球囊斩获美国食品药品监督管理局(FDA)上市许可……
作为国家战略核心承载区,浦东肩负着打造世界级生物医药产业集群的使命,持续提升创新策源能力,全球首创(First-in-class)、中国首发(First-in-China)、临床首用(First-in-Human)的“3F”创新产品持续涌现。
今年以来,首创、首发、首证新品持续落地浦东,全球前沿创新药械、高端技术与项目加速落地集聚浦东,本土龙头企业的创新研究成果与核心产品同步加快迈向国际市场,生物医药领域双向开放的节奏愈发强劲。
葛兰素史克突破临床治疗困境
近日,葛兰素史克宣布中国国家药品监督管理局已批准倍乐锐®(注射用玛贝兰妥单抗)与硼替佐米和地塞米松(BVd)联合用于治疗既往接受过至少一线治疗的多发性骨髓瘤成年患者。
据悉,该获批的上市申请被纳入了优先审评审批程序,BVd联合治疗方案有望相比现有疗法带来显著的疗效改善,该治疗方案被纳入突破性治疗药物程序。值得一提的是,倍乐锐®可在多种治疗场景中以30分钟的门诊输注方式满足患者多样化的治疗需求。
葛兰素史克高级副总裁、全球肿瘤研发负责人表示:“多发性骨髓瘤患者在复发后,亟需兼具疗效与可及性的治疗选择。此次倍乐锐®在中国获批,其差异化的作用机制有望延缓疾病进展、延长患者生存期。此外,作为目前唯一的抗BCMA抗体偶联药物(ADC),倍乐锐®可全程在门诊使用,无需复杂的用药前准备方案或住院治疗,可在不同治疗场景下使用。”
葛兰素史克副总裁、中国总经理余慧明表示:“我们希望通过倍乐锐®的获批,为突破这一血液肿瘤的临床治疗困境打开全新路径,助力进一步提升多发性骨髓瘤患者生存率。葛兰素史克将携手各方、积极探索,为减轻患者用药负担和提升药物可及性不懈努力。”
复宏汉霖公布7项创新成果
与此同时,复宏汉霖在近期举行的美国癌症研究协会年会上,集中公布7款创新管线的最新临床前数据。此次展示的创新成果依托公司前沿开发平台,全面覆盖了极具开发潜力的前沿靶点。
研究数据显示,其中多款候选分子在临床前的头对头比较中展现出同类最优(Best-in-class, BIC)或同类首创(First-in-class, FIC)的治疗潜力。例如,复宏汉霖发布的TCE平台,通过同时提供CD3激活信号(第一信号)与CD28共刺激信号(第二信号),显著增强了T细胞在免疫抑制性肿瘤微环境中的持久杀伤能力。
在抗体偶联药物(ADC)的设计中,高毒性载荷虽然能有效杀伤肿瘤细胞,但也严重限制了临床给药剂量,使其难以达到最佳抗体水平,导致治疗窗口狭窄。为突破这一技术瓶颈,复宏汉霖自主开发了新一代ADC技术平台Hanjugator™,该平台在“抗体介导的信号阻断/内化功能”与“小分子毒素的强效杀伤功能”之间找到最优平衡,实现1+1>2的治疗效果。
在深耕前沿技术平台的同时,复宏汉霖亦在持续探索具备突破性作用机制的创新分子。HLX43是一款具有潜在同类最优(Best-in-class)特征的广谱抗肿瘤PD-L1 ADC,兼具免疫检查点阻断与载荷介导细胞毒性的作用机制。目前,复宏汉霖拥有50余项处于早期阶段的创新资产,其中约70%具备同类最佳(Best-in-Class)潜力,并在全球同步推进30余项临床研究。
微创®冠脉新一代球囊获FDA上市许可
同样传出好消息的还有位于浦东的上海微创医疗器械(集团)有限公司,其自主研发的Firefighter™ Pro/热火战士™ Pro冠脉球囊扩张导管,成功获得美国食品药品监督管理局的510(k)上市许可。
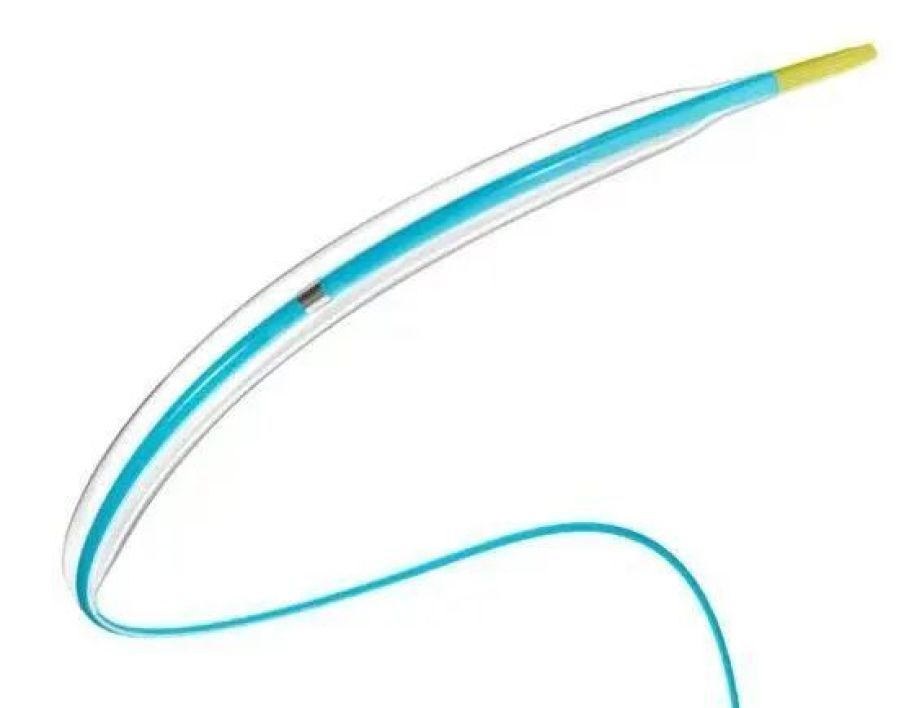
微创®冠脉多款产品相继获批,不仅丰富了在美国市场的产品组合,更体现了公司在研发体系、质量管理及临床转化能力上已接轨国际顶尖标准。相关经验的沉淀,将为后续产品注册提供可复用的路径。
记者了解到,在此基础上,该公司正加速推进腔内影像设备、药物支架等核心产品的FDA注册进程,逐步构建“精准影像评估-病变高效处理-支架植入治疗”的全链条冠脉介入整体解决方案,美国市场布局已从“单个产品突破”进入“多产品协同推进”新阶段。