
基因与细胞治疗正处于疾病创新性治疗手段的最前沿,成为肿瘤、代谢性疾病、遗传病等多类重大疾病的重要突破口,有望显著提升临床疗效并改善患者生活质量。然而,传统细胞与基因治疗在实际临床应用中仍面临诸多挑战,例如给药方式复杂、体内调控精度不足以及患者长期治疗依从性较低等问题。这些瓶颈在一定程度上制约了相关技术从实验室走向临床转化。在此背景下,如何实现对“活体药物”的个性化、精准化和可控化调节,成为医学界、产业界和学术界共同关注的前沿难题。
阿洛酮糖是一种天然存在的稀有单糖,已被美国食品药品监督管理局(FDA)认定为“普遍认为安全(GRAS)”的食品成分。其甜度约为蔗糖的70%,热量极低,血糖生成指数接近于0,并被认为具有辅助调节血糖和脂质代谢的潜在益处,因此广泛应用于无糖食品和饮料中。2025年,我国国家卫生健康委员会亦正式批准阿洛酮糖作为新食品原料,为其在健康与生物医学领域的应用奠定了政策基础。
基于这一安全、可口且易于摄入的天然甜味剂,2026年1月4日,上海市同济医院(同济大学附属同济医院)乳腺外科中心蔡丰丰主任医师、乔龙亮博士后联合华东师范大学生命科学学院首批尚思探索学者叶海峰教授,以及上海大学医学院王美艳研究员,在国际知名学术期刊Advanced Science(Q1,影响因子14.1)上以研究长文(Research Article)形式发表题为 “A Natural Sweetener-inducible Genetic Switch Controls Therapeutic Protein Expression in Mammals” 的论文(图一)。该研究从“智能活体药物”的设计理念出发,成功构建了一种由天然甜味剂D-阿洛酮糖触发的人工基因开关系统——PURE系统。该系统能够在哺乳动物体内实现对治疗性蛋白表达的远程、可逆且剂量依赖式调控。研究表明,通过口服含阿洛酮糖的饮料(如特定配方的可乐),即可精准“开启”或“调节”工程化细胞中目标蛋白的表达水平,从而实现一种“可饮用触发”的细胞治疗新策略。

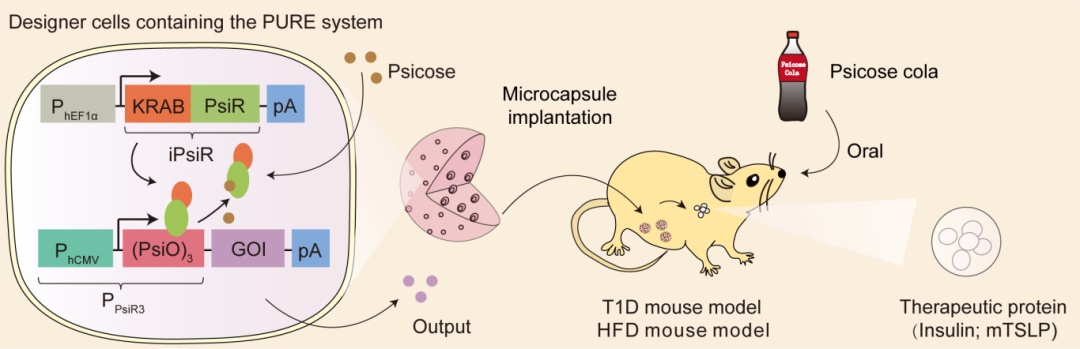
图一. 文章概念图
具体内容:
PURE 系统以来源于土壤农杆菌(Agrobacterium tumefaciens)的转录因子 PsiR为核心调控元件。研究团队通过理性设计结合人工智能(AI)辅助的定向进化策略,对PsiR进行系统性优化,使工程化细胞能够以极高的灵敏度和特异性识别天然甜味剂阿洛酮糖信号,从而实现对治疗基因表达的精准“开启”与“关闭”(图一)。
在此基础上,研究人员创新性地将阿洛酮糖引入为一种安全、可口且可控的“治疗触发器”,并首次提出并验证了“通过饮用可乐即可调控细胞治疗”的概念性方案。作为概念验证,在动物实验中,研究团队将搭载PURE系统的工程化细胞进行微囊化并植入小鼠体内,用于代谢性疾病的精准控制及未来肿瘤特异性杀伤。
该系统具有高度特异性、可逆性和良好的生物安全性,同时显著提升了治疗的可控性与生活方式兼容性。研究人员表示,这种“食品级触发-细胞级响应”的策略,有望为肿瘤合并代谢性疾病提供更加安全、便捷、个性化的治疗新路径。该研究不仅为活体药物和精准治疗提供了新的技术范式,也展示了合成生物学在连接日常生活与前沿医学之间的巨大潜力。未来,相关技术有望进一步拓展至实体肿瘤等多种疾病领域,为活体细胞治疗的临床转化奠定基础。

图二. 文章封面图:通过一只喝“可乐”的小鼠,形象地表现出研究中提出的“喝饮料即可启动细胞治疗”的概念。人工定制可乐能够激活体内植入的“智能细胞”,让它们分泌治疗蛋白。画面整体温暖、自然,象征这种疗法安全、可控、生活化。
近年来,同济医院乳腺外科中心蔡丰丰团队利用合成生物学手段在乳腺癌疾病治疗领域进行开创性的工作并发表系列高质量学术论文。
2025年3月17日,蔡丰丰团队在国际知名期刊《Nature Cancer》(Q1,影响因子:28.5)发表研究论文:Engineered bacteria for near-infrared light-inducible expression of cancer therapeutics,开发了一种能够响应近红外光的新型光遗传学工具——NETMAP系统,并将其上载到减毒沙门氏菌中,将其武装成“光控溶瘤战士”,在人源乳腺癌模型中实现了对乳腺癌的治疗,为乳腺癌精准治疗领域提供了创新性的解决方案,具有潜在的临床转化价值。
2025年7月6日,在国际知名期刊《Advanced Science》(Q1,影响因子:14.1)发表研究论文:Optogenetic-controlled iPSC-based vaccines for prophylactic and therapeutic tumor suppression in mice,开发了一种高效、灵敏响应红光的新型光遗传学工具——RID系统,利用睡美人转座技术稳转到干细胞基因组中,将其改造成智能光控干细胞疫苗,成功实现对乳腺癌的预防,为癌症的精准预防领域提供了创新性的解决方案,具有潜在的临床转化价值。这种创新方案为乳腺癌精准预防提供了潜在的临床应用价值,研究团队正在积极推动该成果进入临床阶段,从而造福广大潜在患癌患者。
文章链接:
L. Qiao, Z. Wang, S. Tang, et al. “A Natural Sweetener-inducible Genetic Switch Controls Therapeutic Protein Expression in Mammals.” Advanced Science (2026): e14226. https://advanced.onlinelibrary.wiley.com/doi/10.1002/advs.202514226.
图文|乳腺外科中心
编辑|张鹰妮
责任编辑|谢壮丽